Der Einfluss von Metallionen in der HPLC ist schon seit Längerem bekannt; sprechen wir eher von einem zwar vorhandenen, jedoch bis dato bei vielen Anwender:innen weniger sich stark im Focus befindenden Problem. In den letzten Jahren erlebt dieses Thema allerdings aufgrund der zunehmenden Wichtigkeit von Biomolekülen eine gewisse Renaissance.
Um welche Metallionen handelt es sich?
Wo kommen sie her und was bewirken sie?
Sind sie vermeidbar? Und: Können sie entfernt werden?
Doch bevor wir uns dem Thema widmen, zunächst ein kleiner semantischer Exkurs:
Konfusion von Begrifflichkeiten
Begriffe im hiesigen Zusammenhang werden nicht von allen Beteiligten einheitlich verwendet. Dadurch entsteht eine gewisse Konfusion. Nachfolgend eine kurze Einordnung, wobei diese weder den Anspruch auf Vollständigkeit erhebt, noch kann ich erwarten, dass alle mit dieser 100 % d’accord gehen.
- Bioinert; geringe Wechselwirkungen mit Hardware-Komponenten, geringes Risiko für carryover; ältester Begriff, bereits 1933 verwendet: Aluminium-Oberfläche als Alternative zu Eisen. Im Umfeld der HPLC sind die verwendeten Materialien hier Titan, Keramik, PEEK
- Biokompatibel; keine Korrosionsgefahr trotz Chlorid-Ionen im Eluenten; oft synonym bzw. gleich zu setzen mit Bio-LC und Stainless steel-free; verwendete Materialien: Titan und spezielle Legierungen, z. B. MP35N
- Metall-frei; verwendete Materialien: PEEK, Saphir
Weitere anzutreffende Attribute sind: „Inert“, „truly bioinert“ (PEEK), schließlich „fully biocampatible“.
Treffsichere Bezeichnungen wären eher: „Low Adsorption Materials“ bzw. „Corrosion Resistant Materials“ – aber das ist eine persönliche Ansicht.
1. Wo kommen sie her?
- Bei älteren stationären Phasen befinden sich Schwermetallionen als Kontaminationen in der Kieselgel-Matrix. Das verwendete Kieselgel der ersten Generation ist natürlichen Ursprungs und unterliegt demnach natürlichen Schwankungen. Somit befinden sich Schwermetallionen, aber auch K, Na, Ca, Al etc. im Kieselgel-Gerüst, siehe Abbildung 1
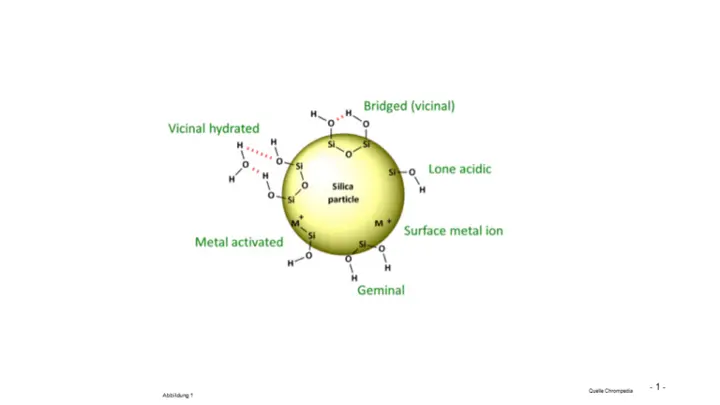
Abbildung 1
Metallionen im Kieselgel für die HPLC
- Alle in der HPLC verwendeten Lösungsmittel waschen Metallionen aus metallisch-verbauten Teilen in der Anlage aus, siehe Abbildung 2-4
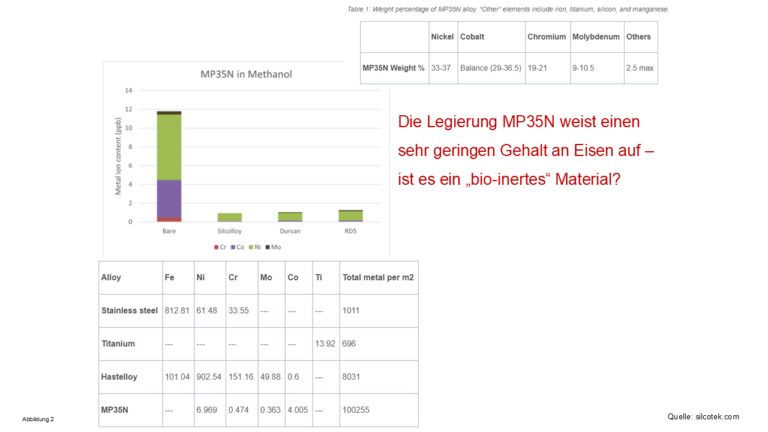
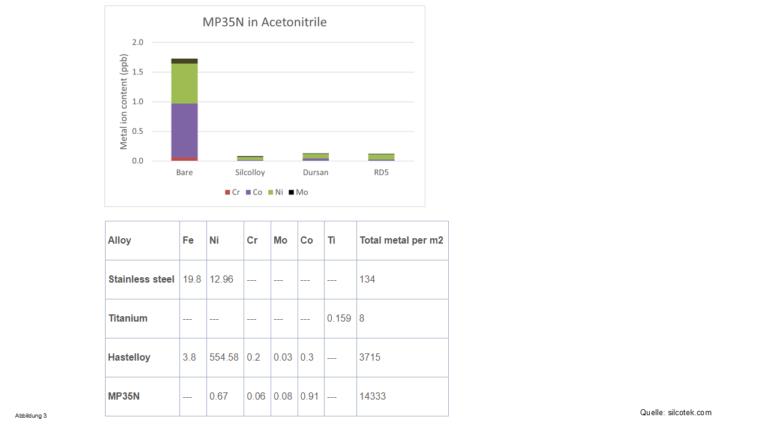
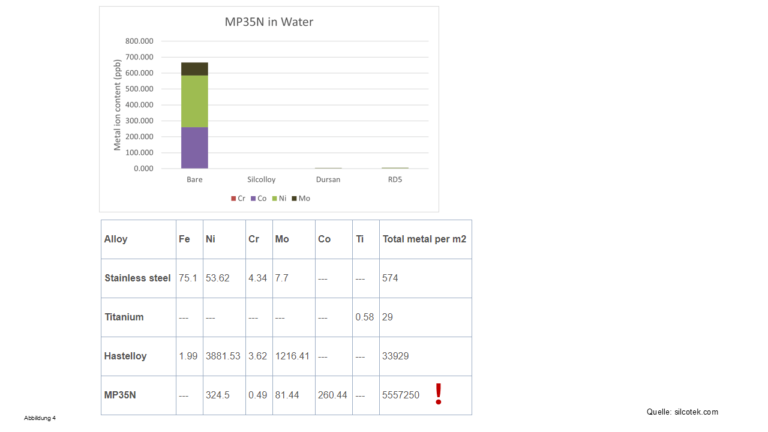
Abbildung 2-4 Metallionen, die von HPLC-Lösungsmitteln herausgewaschen werden
– Auch das harmlos anmutende Wasser wäscht „ordentlich“ Metallionen
aus
– Auch das harmlos anmutende Wasser wäscht „ordentlich“ Metallionen
aus
– Die Legierung MP35N enthält zwar keine Eisenionen, aber die anderen
darin erhaltenen Metallionen werden von allen Lösungsmitteln herausgewaschen – speziell von Wasser, siehe in Abbildung 4
die ausgewaschene Menge an Metallionen! Kann man bei Verwendung eines derartigen Materials in einer HPLC-Anlage
von „Bio-LC“ sprechen? (Bio)Moleküle können ja auch mit anderen Metallionen außer Eisen komplexieren!
- Metallionen kommen zusammen mit der Probe in das Gerät und gelangen damit zur Säule, wo sie in/an der stationären Phase adsorbiert werden. Man denke nur an Kontrastmittel (Barium, Gadolinium) und Zytostatika (Platin-Ionen)
2. Was bewirken sie? Nachfolgend einige Beispiele:
- Metallionen an der Kieselgel-Oberfläche können zum einen Metall-Komplexe bilden, siehe Abbildung 1 und 5. Sich im Inneren der Kieselgel-Matrix befindenden Schwermetallionen üben zum anderen einen -I-Effekt auf die Silanolgruppen aus (sie ziehen von ihnen Elektronen ab) und begünstigen dadurch die Bildung von dissoziiert (ionisch) vorliegenden und somit „aggressiven“ Silanolen. Solche können mit basischen Molekülen Ionenaustausch-Wechselwirkungen eingehen, Ergebnis: Chemisches Tailing. Wir haben weiter oben gesehen, dass die älteren Kieselgele eine beträchtliche Menge an Metallionen als Kontaminationen enthalten. Das ist der Grund, warum bei älteren Säulen trotz Verwendung eines sauren Eluenten immer wieder chemisches Tailing auftaucht – es klappt bei solchen Materialien kaum, „aggressive“ Silanole zu vermeiden
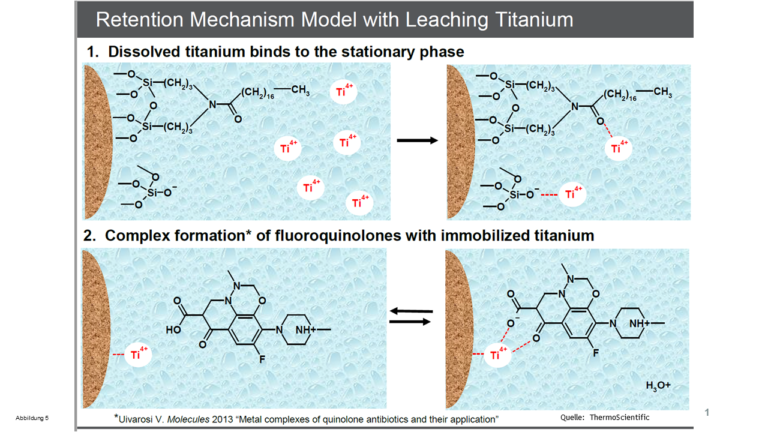
Abbildung 5 – Einfluss von Metallionen in der Kieselgelmatrix
- Biomoleküle, aber auch andere Moleküle (Lewis Basen, Säuren) werden teilweise an Metalloberflächen adsorbiert, Ergebnis: Keine reproduzierbaren Peakflächen, starkes Tailing, in Worst Case totale Adsorption (Memory-Effekt, carryover)
- Fe2+-Ionen können Komplexe bilden (Carboxylate, N-haltige Substanzen mit einem freien Elektronenpaar am Stickstoff), ferner wirken sie katalytisch bei einer Reihe von Reaktionen
- Durch Fe2+-Ionen können Chinone zu Katecholaminen reduziert werden
- Es besteht generell die Gefahr, dass in einer HPLC-Anlage – vor allem bei einer häufigen Verwendung von Puffern – ein Biofilm entsteht. Aus Bakterien entstehen Zuckerverbindungen, die wiederum eine Polymermatrix bilden. Diese „saugt“ (auch) Schwermetall- und Alkalionen auf; durch die Biomineralisation entsteht eine harte Plaque, die schwer zu entfernen ist. Ergebnis: Tailing und/oder „Buckel“
3. Sind sie zu vermeiden?
Wohl kaum: So lange Lösungsmittel mit metallischen Oberflächen – welche auch immer – in Berührung kommen, werden Metallionen in bestimmter Konzentration ausgewaschen. Es kommt auf die Moleküle an, inwieweit dieser Vorgang schlimm ist. In der Zwischenzeit gibt es schon mit einer PEEK-Ummantelung versehene Säulen (Druckstabilität?) bzw. beschichtete Säulen, z. B. amorphes Glas. Die Moleküle „sehen“ in der Säule demnach keine Metall-Oberfläche – aber eben, nur in der Säule. Und merke in diesem Zusammenhang: Je größer die (spezifische) Oberfläche ist, umso mehr Metallionen werden aus dieser ausgewaschen, so verdient beispielsweise die Fritte besondere Beachtung. Es sind zwar seit einiger Zeit Bestrebungen im Gange, aber bis dato gibt es (noch) keine kommerziell erhältlichen, vollständig metallfreien HPLC-Anlagen.
4. Können sie (vollständig) entfernt werden?
Auch hier lautet die Antwort: Wohl kaum. Natürlich sind Spülprozeduren mit EDTA und Phosphor-/Oxalsäure usw. bekannt und beschrieben worden. Abgesehen von praktischen Problemen, ist ein derartiger Schritt zwar hilfreich, aber er kann nie zu einer vollständigen und vor allem nachhaltigen Entfernung von Metallionen führen. Kann man Metallionen in der Apparatur denn nicht wenigstens „verstecken“? Ja schon, auch das ist möglich, aber dies stellt schwerlich eine zufriedenstellende Lösung auf Dauer dar: Passivieren mit 6 N HNO3 hilft definitiv eine Zeit lang – aber eben: Eine Zeit lang. Die Prozedur ist etwas aufwendig und müsste 2–3-mal im Jahr wiederholt werden. Also, passivieren: Vielleicht, hilfsweise, u.U., evtl. und als „Ultima Ratio“ schon überlegenswert. Die Entfernung eines möglichen Biofilms ist eine Sache für sich, damit werden wir uns in einem zukünftigen HPLC-Tipp befassen.
Wir haben die ganze Zeit auf die „armen“ Metallionen eingedroschen. Gibt es denn nichts Positives über sie zu sagen? Doch schon: Man kann bestimmte chirale Säulen bewusst mit Cu2+– oder Cd2+-Ionen belegen. Diese Kationen bilden mit den chiralen Selektoren auf der Oberfläche des Materials und den zu trennenden Enantiomeren große Komplexe. Acetonitril-Moleküle bedingen eine Chelatstabilisierung, es ergibt sich eine hervorragende Enantioselektivität („Ligandenaustausch-Chromatographie“). Aber ich muss zugeben, das hier ist schon etwas Spezielles…
© Dr. Stavros Kromidas
Weitere Tipps von diesem Jahr finden sich unter: https://www.kromidas.de/hplc-tipps-des-jahres/

